Crohn-betegség - Okok, tünetek, kezelési lehetőségek

Mi a Crohn-betegség?
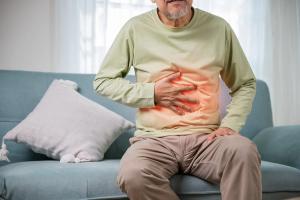
A Crohn-betegség egy gyulladásos bélbetegség (IBD), ami hasi fájdalomhoz, súlyos hasmenéshez, krónikus fáradtsághoz, súlyvesztéshez és alultápláltsághoz vezethet. A gyulladás az emésztőrendszer különböző területeit érintheti (legtöbbször a vékonybél utolsó szakaszát vagy a vastagbelet), és akár a bélfal mélyebb rétegeibe is kiterjedhet. A betegség jelentős fájdalommal járhat, és kedvezőtlenül hathat az életminőségre. Súlyosabb esetekben akár életet veszélyeztető szövődmények is kialakulhatnak. A kutatók jelenleg még nem tudják, mi az oka, kiket érinthet leginkább, és mi a legjobb kezelési módja. Az elmúlt évtizedek jelentős kezelési eredményei ellenére, még ma sincs rá gyógymód. A Crohn-betegség kapcsán tehát további kutatások szükségesek. Bár a Crohn-betegségnek nincs ismert gyógymódja, különböző terápiák csökkenthetik a tüneteit, sőt, hosszabb tünetmentes időszakokat, valamint a gyulladás mérséklődését is támogathatják. A megfelelő kezeléssel az érintett betegek életminősége jelentősen javulhat. 1
A Crohn-betegség funkcionális orvoslási megközelítése tartalmazza a gyulladás kiváltó okának feltárását és kezelését a test természetes gyógyító mechanizmusainak a támogatásával. A funkcionális, vagy integratív orvos ételintolerancia tesztet, székletvizsgálatot, és egyéb, egyénre szabott, betegspecifikus teszteket kérhet. Ezek segítségével, a beteggel együttműködve azonosíthatja a gyulladás kiváltó okát, és így személyre szabott kezelési tervet, és étrendet tud összeállítani.
Mik a Crohn-betegség tünetei?
Sok Crohn-beteg már évekkel a hivatalos diagnózis felállítása előtt tapasztal tüneteket 2. A panaszok leggyakrabban a tizen- vagy huszonéves életkorban jelentkeznek, de a betegség bármely életkorban kialakulhat 3. A Crohn-betegségre jellemző a hullámzó lefolyás, amelyet váltakozó fellángolások és tünetmentes időszakok (remissziók) jellemeznek. 4 A betegség tünetei többnyire fokozatosan jelentkeznek, bár ritkán, de előfordulhatnak hirtelen fellépő panaszok is. Bizonyos tünetek az idő múlásával súlyosabbá válhatnak. A leggyakoribb kezdeti tünetek a következők 5:
- hasmenés
- hasi görcsök
- véres széklet
- láz
- fáradtság
- étvágytalanság
- fogyás
- székletürítés utáni további teltségérzet
- gyakori székletürítési inger
Ezeket a tüneteket gyakran össze lehet téveszteni az ételmérgezés, gyomorrontás, vagy allergia tüneteivel.

1. ábra.: A Crohn-betegség legkorábbi tünetei a hasfájás, a székrekedés, a gyomorgörcsök, a fogyás, a láz és a fáradtság lehetnek
A hasi fájdalom a Crohn-betegség egyik leggyakoribb korai tünete 6, különösen a has jobb alsó területén jelentkezik. Súlyosabb esetekben a betegek akár napi több, mint 20 bélmozgást is tapasztalhatnak, és gyakran az éjszaka folyamán is fel kell kelniük székletürítésre 3, 6–8. Véres széklet is előfordulhat, amely jellemzően időszakos, színe világos- vagy sötétvörös. Előrehaladottabb állapotban akár jelentős mennyiségű vérzés is kísérheti. 9 A betegség előrehaladtával a tünetek egyre súlyosabbá válhatnak. Ezek közé tartozhatnak az alábbi, kifejezettebb panaszok 5:
- végbélsipoly
- fekélyek, melyek a szájtól a végbélnyílásig bárhol előfordulhatnak
- az ízületek és a bőr gyulladása
- légszomj, vagy vérszegénység miatti csökkent mozgásképesség
A betegség korai felismerése segíthet elkerülni a súlyosabb szövődményeket, és lehetővé teszi a kezelés korai megkezdését. A Crohn-betegség nemcsak a bélrendszert érinti, hanem a test más területein is megjelenhetnek hozzá kapcsolódó tünetek, például a következők 10:
- szem (vörös szemek, fájdalom és/vagy látászavarok)
- száj (sebek)
- ízületek (duzzanat és fájdalom)
- bőr (dudorok, fekélyek, sebek, kiütések)
- csontok (csontritkulás)
- vese (vesekő)
- máj (primer szklerotizáló cholangitis és cirrhosis) - ritka esetben

2. ábra.: A Crohn-betegséghez kapcsolódó tünetek a bélrendszeren kívül, a test egyéb részein is jelentkezhetnek
A emésztőrendszeren kívül jelentkező tüneteket a Crohn-betegség extraintesztinális manifesztációinak nevezik. Van akinél ezek a Crohn-betegség első tünetei, melyek még évekkel a bélrendszeri panaszok előtt jelennek meg. Másoknál a bélrendszeri tünetek fellángolása idején jelennek meg csak.
A Crohn-betegség szövődményei
A Crohn-betegség szövődményei közé tartozhat a bélelzáródás, a tályogképződés, a bélperforáció és a vérzés, amelyek bizonyos esetekben életveszélyesek lehetnek. A Crohn-betegség, mint az már említésre került, nem csupán a gasztrointesztinális traktust érinti, hanem több más szervrendszerre is hatással lehet 11. A szemet érintő egyik gyakori gyulladásos szövődmény az uveitis, amely homályos látást és szemfájdalmat okozhat 12. Kezelés hiányában akár vaksághoz is vezethet 11. Gyulladás kialakulhat a szemfehérjében, tehát a kötőhártyában és az ínhártyában is, ami scleritishez vagy episcleritishez vezethet. 12 A Crohn-betegség kapcsolatban állhat a szeronegatív spondylarthritis nevű reumatológiai betegséggel is, amelyet ízületi gyulladás (arthritis) vagy az inak tapadási pontjain kialakuló gyulladás (enthesitis) jellemez. 12 További érintett rendszerek lehetnek a bőr, a vérképző rendszer, valamint az endokrin rendszer. A leggyakoribb bőrelváltozás a Crohn-betegek körében az erythema nodosum, amely az érintettek mintegy 8%-ánál fordul elő. Ez a bőrprobléma fájdalmas, vörös csomókkal jelentkezik leggyakrabban a lábszáron 12–14. Egy ritkább, de súlyosabb bőrbetegség a pyoderma gangrenosum, amely a betegek kevesebb mint 2%-ánál alakul ki, és fájdalmas, fekélyes csomókkal jár. 11, 14 A Crohn-betegség fokozza a vérrögképződés kockázatát is 12. A lábszár duzzanata és fájdalma mélyvénás trombózisra, míg a hirtelen fellépő nehézlégzés tüdőembóliára utalhat. Neurológiai szövődmények is előfordulhatnak, amelyek a betegek akár 15%-át is érinthetik. Ezek közé tartoznak a rohamok, stroke, izombántalmak (myopathia), perifériás neuropátia, fejfájás és depresszió. 15 A gyulladásos folyamatok miatt a Crohn-betegség növelheti a daganatos megbetegedések kockázatát is. Azoknál, akiknél a vékonybél érintett, megnő a vékonybélrák kialakulásának valószínűsége 16, míg a vastagbél érintettsége esetén fokozott a vastagbélrák kockázata. 17 A Crohn-betegeknél gyakran alakul ki vérszegénység, amely lehet B12-vitamin-, folsav-, vashiány vagy krónikus gyulladásos állapot következménye 18–19. A betegség leggyakrabban a terminális ileumot, azaz a vékonybél utolsó szakaszát érinti, ahol a B12-vitamin felszívódik 18. Ez a magyarázata, hogy a B12-hiány különösen gyakori azoknál, akiknél ezt a bélrészt műtétileg eltávolították. 19
Mik a Crohn-betegség okai?
Bár a Crohn-betegség pontos okai ismeretlenek, feltehetően a genetikailag fogékony egyének környezeti-, immun- és bakteriális tényezőinek kombinációja okozza 6, 20–22. Tehát az alábbiakban bemutatott okoknak (genetika, immunrendszer, kórokozók, környezeti hatások) mind szerepe lehet a betegség kialakulásában. Nem azonosítható egy olyan faktor, mely önmagában okozza a kórképet.
Genetika
A Crohn-betegség kialakulása valószínűleg a genetikai hajlam és a környezeti faktorok kombinációjának köszönhető 23. Ez az első olyan genetikailag összetett kórkép, melyben a genetikai tényezők és az immunrendszer közötti kapcsolatot részleteiben feltárták 24. Több mint 70 génről mutatták ki, hogy szerepe lehet a betegség kialakulásában, a teljes kockázat fele kapcsolódik a genetikához. 3, 25 A genom egészére kiterjedő asszociációs vizsgálatok kimutatták, hogy a gyulladásos bélbetegségek genetikailag kapcsolatban állnak a lisztérzékenységgel 26. A Crohn-betegséget az LRRK2 génhez is kapcsolják, ami a Parkinson-kórral is kapcsolatban van. 27
Immunrendszer
Az uralkodó nézet szerint a Crohn-betegség egy autoimmun betegség. Más elméletek a veleszületett immunitás károsodását gyanítják a betegség hátterében 28. Egy hipotézis szerint a makrofágok károsítják a citokin-szekrécióját, amely hozzájárul a veleszületett immunitás károsodásához, és így vezet egy tartós mikrobák által kiváltott gyulladásos válaszhoz 21, 29. Egy másik teória szerint a Crohn-betegség által okozott gyulladást egy túl erős Th1 és Th17 immunválasz okozza. 30–31 Egy másik feltételezés szerint az immunrendszer a testben lévő parazitáknak köszönhetően alakul ki. Napjaink szigorú higiéniájának következtében azonban ezekkel nem találkozik a szervezet és így az immunrendszer legyengül. Ennek igazolására, tesztalanyokat ártalmatlan parazitáknak tettek ki, melyre a Crohn-betegek szervezete kedvezően reagált: 29-ből 23 beteg esetében pozitív változás történt, köztük 21 alanynál teljes remisszió volt tapasztalható. 32
Kórokozók
Bár a Crohn-betegség pontos kiváltó okai nem ismertek, egyre több kutatás támasztja alá, hogy a genetikai hajlam mellett különféle mikroorganizmusok, köztük kórokozók is szerepet játszhatnak a betegség kialakulásában. A jelenlegi elméletek szerint a Crohn-betegség olyan egyéneknél jelenik meg, akiknél a bélflórával szemben kóros immunválasz alakul ki 33. Ezt a válaszreakciót kiválthatja egy korábbi fertőzés, például gasztroenteritisz, vagy a bélmikrobiális egyensúly (homeosztázis) megbomlása, azaz diszbiózis 3.
Mikrobiom
A bélmikrobiom, amely az emésztőrendszerben élő mikroorganizmusok – főként baktériumok – összességét jelenti, kulcsszerepet tölt be a tápanyagok lebontásában és felszívódásában, az immunrendszer szabályozásában, valamint a bélnyálkahártya épségének fenntartásában. Crohn-betegségben ez az egyensúly megbomlik: csökken a mikrobiális diverzitás, és eltolódik az arány a jótékony hatású baktériumok rovására. Ilyen gyulladáscsökkentő törzsek például a Faecalibacterium prausnitzii, Bifidobacterium és Lactobacillus fajok, amelyek mennyisége jelentősen visszaesik 34. Ezzel párhuzamosan megnő a potenciálisan patogén mikroorganizmusok aránya, különösen a Proteobacteria törzsbe tartozó fajoké, mint az Escherichia coli vagy a Shigella dysenteriae. 35–36 Kiemelt figyelmet kapnak az adherens-invazív E. coli (AIEC) törzsek, amelyek képesek megtapadni a bélhámsejteken, behatolni azokba, és makrofágokon belül szaporodni, ezáltal fokozva a gyulladásos válaszreakciót 37. Az adatok szerint a Crohn-betegek körülbelül egyharmadánál kimutatható AIEC jelenléte 38. A mikrobiom összetételének változásai ráadásul nemcsak a betegség fennállásával, hanem annak súlyosságával is összefüggést mutatnak: például az Alistipes shahii és Pseudodesulfovibrio aespoeensis jelenléte alacsonyabb gyulladási aktivitással jár, míg a Polynucleobacter wianus fokozott gyulladással és súlyosabb kórlefolyással kapcsolatos. Kutatások szerint az Alistipes shahii egyes anyagcseretermékei akár tumorgátló hatással is bírhatnak, míg az Akkermansia muciniphila immunmoduláló hatásán keresztül, többek között IL-10-et termelő regulátoros T-sejtek aktiválásával, csökkentheti a gyulladásos citokinek és kemokinek – például TNF-α, IL-1β, IL-6 – szintjét a szervezetben. Ezzel szemben olyan opportunista kórokozók, mint a Morganella morganii és a Proteus mirabilis, szintén túlszaporodnak diszbiózis esetén, és a bélnyálkahártyát károsítva fenntartják a gyulladásos állapotot. A M. morganii különösen azért figyelemre méltó, mert indoliminek termelésével DNS-károsodást idézhet elő, így hozzájárulhat a vastagbélrák kialakulásához is 39. Fontos hangsúlyozni, hogy a mikrobiom egyensúlyának megbomlása nem pusztán következménye a gyulladásnak, hanem aktívan hozzájárulhat annak kiváltásához és fenntartásához is. Ez a felismerés új terápiás lehetőségeket nyit meg, például probiotikumok, prebiotikumok, mikrobiom-transzplantáció vagy mikrobiom-moduláló növényi hatóanyagok alkalmazása irányában.
Egyéb mikroorganizmusok
A bélbaktériumokon túl azonban más mikroorganizmusok is felmerültek, amelyek önálló kóroki szerepet tölthetnek be. A jelenlegi bizonyítékok alapján potenciális szereplőként szóba jöhet a Mycobacterium avium subspecies paratuberculosis (MAP), bizonyos patotípusú E. coli-törzsek (pl. AIEC), az Epstein–Barr vírus (EBV), a Candida tropicalis és a Clostridioides difficile. Ezek a kórokozók képesek közvetlenül károsítani a bélnyálkahártyát, és fokozhatják az immunrendszer téves vagy túlzott aktivációját, így hozzájárulhatnak a Crohn-betegség kialakulásához és krónikus fennmaradásához. Mycobacterium avium subspecies paratuberculosis (MAP) A MAP a szarvasmarhák gyomrában Johne-betegséget okoz. Mivel a Johne-betegség hasonlít a Crohn-betegségre, feltételezik, hogy a Crohn-betegséget is ez a baktérium okozhatja. Több tanulmány is vizsgálta a baktérium szerepét a Crohn-betegség kialakulásában. 40–41 Terápiás lehetőségként a MAP elpusztítását is vizsgálják 42. Megvizsgálták például a MAP antibiotikumokkal történő kezelését. Az eredmények ugyan nem egyértelműek, de feltételezik, hogy az antibiotikumok használata előnyös. 43–44 Escherichia coli Mivel az AIEC (adherens-invazív) E. coli gyakoribb a Crohn-betegségben szenvedők szervezetében, az adherens-invazív E. coli specifikus törzseit is kapcsolatba hozták betegséggel 37, 45–46. Ezek a baktériumok erősebb biofilmet képesek létrehozni a nem adherens-invazív E. coli törzsekhez képest. 47–48 Epstein-Barr vírus Az Epstein-Barr vírus szorosan kapcsolódik számos bélrendszeri betegséghez. A Crohn-betegségen kívül társítják a colisits ulcerosához, a peptikus fekélybetegséghez, az akut vakbélgyulladáshoz és a gyomorrákhoz. Egészséges gyomor-bél nyálkahártyában nem található meg az Epstiein-Barr vírus, de a Crohn-betegségben szenvedők bélrendszerében 55%-63%-ban fellelhető. 49–50 Különösen problémás, hogy az Epstein-Barr vírus szunnyadhat, amíg immunszupresszáns gyógyszerek (pl., szteroidok) aktiválják 51. Így ezek a gyógyszerek tovább súlyosbíthatják a Crohn-betegséget. 52 Candida tropicalis Egy 2016-os, az American Society for Microbology c. folyóiratban megjelent tanulmány megemelkedett Candida tropicalis előfordulást mutatott ki a Crohn-betegségben szenvedő betegek székletében. A gombának magas arányát találták a Saccharomyces cerevisiae antitestek mellett is, így ez egy módja annak, hogy megkülönböztessük a Crohn-betegséget a fekélyes vastagbélgyulladástól (colitis ulcerosa). Ezeket a gombákat két baktériummal: E.coli és S.marcescens együtt fedezték fel. A gomba, és a két baktérium együtt vastag, nagy biofilmet alkottak. Ezek a biofilmek hozzájárultak a bélflóra egyensúlyának zavarához (diszbózishoz) a Crohn-betegségben. Ez a tanulmány mutatta ki először hogy gomba is lehet a Crohn-betegség oka. Korábban csak baktériumokat, és vírusokat feltételeztek a hátterében. 33 Clostridioides difficile A Clostridium difficile baktérium a bélrendszer gyakori lakója, több törzse létezik, melyek patogenitásukat tekintve egymástól eltérnek. Jelenlétük nem jelent szükségszerűen betegséget. Antibiotikus kezelést követően gyakran sérül a bélflóra, aminek eredményeként nemritkán hasmenés, ill. Clostridium difficile fertőzés jelenik meg. 53 A Clostridium fertőzésnek jelentős szerepe van gyulladásos bélbetegségek esetén is. 54 A Clostridium difficile gyakori kórházi fertőzés, kutatások szerint, mint ilyen, 8-37,2% közötti a mortalitása 55. A fertőzés rizikóját az antibiotikumokkal egyidejűleg adott probiotikus kezelés 50%-al csökkentette. 56
Környezeti hatások
Általánosságban elmondhatjuk, hogy a Crohn-betegség gyakoribb a nyugati világban 57. A Crohn-betegség 1000-ből 3,2 embert érint Európában és Észak-Amerikában 58. Ázsiában és Afrikában kevésbé gyakori. 58–59 A megbetegedés általában tizenéves, vagy huszonéves korban kezdődik, de bármely életkorban kialakulhat 3, 6, 60. A férfiak és a nők körében ugyanolyan gyakori az előfordulása. 6 A Crohn-betegséget az állati-, és a tejfehérje megnövekedett beviteléhez, valamint Omega-6 és Omega-3 többszörösen telítetlen zsírsavak megnövekedett arányához kapcsolják. A növényi fehérjéket fogyasztók között alacsonyabb az előfordulása. A halfehérje fogyasztásával nincs kapcsolatban. 61 Dohányzók körében kétszer nagyobb eséllyel alakul ki Crohn-betegség mint nemdohányzók között. Ráadásul a dohányzás tovább növeli a már meglévő betegség visszatérésének és a fellángolásának rizikóját. 62
A hormonális fogamzásgátlás 1960-as évekbeli bevezetése az Egyesült Államokban a Crohn-betegség gyakoriságának jelentős növekedésével járt. Egy hipotézis szerint ezek a gyógyszerek a dohányzáshoz hasonlóan hatnak az emésztőrendszerre 63. A tartós stresszről is feltételezik, hogy súlyosbítja a betegséget, de konkrét bizonyítékok nincsenek rá. 6
Kockázati tényezők
A Crohn-betegség kiváltó tényezői a következők lehetnek 1:
- Kor: Bár a Crohn-betegség bármely életkorban előfordulhat, a legtöbbször fiatalokon alakul ki. A legtöbb Crohn-betegségben szenvedőt 30 éves kora előtt diagnosztizálják.
- Etnikum: A Crohn-betegség bármelyik etnikai csoportot sújthatja, a legmagasabb előfordulás fehér bőrűek körében van.
- Genetikai tényezők: Nagyobb kockázata van a megbetegedés kialakulásának azok körében, akiknek egy közvetlen hozzátartozója (szülő, testvér, gyermek) Crohn-betegségben szenved. A Crohn-betegséggel élők 20%-ának egy családtagja is a betegséggel él.
- Dohányzás: A dohányzásról való leszokás a legfontosabb kontrollálható kockázati tényező a Crohn-betegség megelőzéséhez.
- Gyulladáscsökkentők: Nem-szteroid gyulladáscsökkentő gyógyszerek használata. Az ilyen gyógyszerek bár nem okoznak Crohn-betegséget, bélgyulladáshoz vezethetnek, ami súlyosbíthatja a betegséget.

3. ábra.: A Crohn-betegségnek olyan kockázati tényezői lehetnek, mint a kor, genetikai tényezők, etnikum vagy a dohányzás
A Crohn-betegség diagnózisa
A Crohn-betegséget nehéz diagnosztizálni 2. Számos teszt elvégzése szükséges a pontos kórmegállapításhoz 60, de sokszor tesztek egész sorával sem lehetséges biztosan felállítani a kórismét. A Crohn-betegség diagnózisának a kórtörténet, a fiziológiai eredményeket, a képalkotó és laboratóriumi vizsgálatok adataira egyben kell épülnie. Fontos megkülönböztetni a Crohn-betegséget az olyan, hozzá hasonló kórképektől, mint például az irritábilis bél szindróma (IBS) vagy Behçet-kór, és az olyan fertőző betegségektől, mint a yersiniózis vagy az enterovírusok. Különös figyelmet kell fordítani az endémiás betegségekre is, mint a tuberkulózis. 3 A következő vizsgálatok lehetnek szükségesek a Crohn-betegség diagnosztizálásához, ill. az IBS-től és a colitis ulcerosától elkülönítéshez, valamint egyéb betegségek kizárásához 3:
- Kórtörténet, köztük a családi kórtörténet elemzése. Itt olyan kérdésekre kell figyelmet fordítani, mint a tünetek kezdetének ideje, közelmúltbeli utazások, vér és/vagy nyálka a székletben, görcsök, éjszakai hasmenés, étkezési szokások, közelmúltbeli bélfertőzések, nem szteroid gyulladáscsökkentő gyógyszerek használata, vakbélműtét, közelmúltbeli gyomor-bélhurut (gasztroenteritis). A bélrendszeren kívüli tünetek szűrése is szükséges.
- Fizikális vizsgálatok: Pulzus, vérnyomás, súly, magasság, testtömeg-index megmérése. Hasi vizsgálat, perianális vizsgálat, rektális digitális vizsgálat és az extraintesztinális tünetek keresése is ide tartozik.
- Mikrobiális vizsgálatok: Székletvizsgálat, Clostridium difficile vizsgálat
- Patológiai és szövettani vizsgálat: Legalább két biopsziás minta szükséges legalább öt szegmensből, beleértve a csípőbélt is.
- Gyomortükrözés
- Vastagbéltükrözés
- Vékonybéltükrözés
- Röntgen
- CT-vizsgálat
- MR-vizsgálat
- Kapszula endoszkópia
- Laboratóriumi vizsgálatok: Teljes vérkép, vörösvérsejt-süllyedés, élesztőgomba antitestek (ASCA) és antineutrofil citoplazmatikus antitestek (ANCA) szűrése, c-reaktív protein szint, elektrolit vizsgálatok, májfunkciós vizsgálatok.
- Akiknél megállapított vagy feltételezett gyomor- bélrendszeren kívüli tünetei vannak, szükséges a konzultáció más szakemberekkel is, mint: sebész, reumatológus, bőrgyógyász, szemész, urológus, nőgyógyász (ha rectovaginális sipoly gyanúja merül fel).
Milyen élelmiszerek okoznak tüneteket?
Gyulladásos bélbetegséget ugyan ételek és italok nem okoznak, de a tüneteket, különösen a fellángolások időszakában, súlyosbíthatják. 1 Hasznos lehet emiatt étkezési naplót vezetni. Az étkezési naplóban nyomon tudják követni a betegek, hogy mit esznek, és azt, hogy étkezés után hogyan érzik magukat. Ennek segítségével megállapítható az, hogy mely ételek okoznak tüneteket. Azok az étrendből eltávolíthatók. Sok gyulladásos bélbetegségben szenvedő azt tapasztalja, hogy a tejtermékek fogyasztásának csökkentésével, vagy teljes megszüntetésével csökkennek a hasmenés, a hasi fájdalom, és a gázképződés tünetei. Felmerülhet még a laktóz-intolerancia, és egyes kutatási eredmények alapján a tejcukor mellett a tejfehérje fogyasztása is problémás. Segíthet, ha nem fogyasztanak kazeint (a tehéntejben található protein) sőt glutént sem. 64 A magasabb rost- és gyümölcstartalmú étrend csökkenti a Crohn-betegség kialakulásának kockázatát, zsírban, többszörösen telítetlen zsírsavakban, húsban és omega-6 zsírsavakban gazdag étrend növelheti. Egyeseknél alacsony rosttartalmú étrenddel kezelhetők az akut tünetek. 65
Milyen szempontok segíthetnek a Crohn-betegségnél?
Nincs olyan gyógymód, vagy műtéti beavatkozás, ami gyógyítja a Crohn-betegséget 3, 6. A kezelés célja tehát a gyulladás csökkentése, a fájdalom, a hasmenés és a vérzés enyhítése, valamint a táplálkozási hiányosságok megszüntetése. 66 A terápia magában foglalhat gyógyszereket, étrend-kiegészítőket, műtétet, vagy mindezek kombinációját. A kezelési lehetőségek attól függnek, hogy a megbetegedés melyik fázisában van a páciens, és mennyire súlyos az állapota. Valamint attól is, hogy a betegségének milyen szövődményei vannak, és hogy a korábbi kezelésekre miként reagált a személy. A Crohn-betegség kezelésére többféle gyógyszert használnak. Ezek közé tartoznak a gyulladáscsökkentők, például a kortikoszteroidok, valamint az antibiotikumok és a hasmenés elleni szerek. Emellett alkalmazhatnak immunszuppresszív szereket, mint a metotrexát vagy azatioprin. A fájdalom enyhítésére különféle fájdalomcsillapítók is szóba jöhetnek. Súlyosabb esetekben biológiai terápiát is bevethetnek. Műtéttel a Crohn-betegség szövődményei (sipolyok, vékonybél elzáródása, vastagbélrák, vékonybélrák, bélelzáródások) kezelhetők. Műtét szükséges abban az esetben is, a ha egy adott bélszakasz már nem reagál a gyógyszerekre 67. Ugyanakkor, a műtétek nem gyógyítják, vagy szüntetik meg magát a Crohn-betegséget. 68 A fáradtságot rendszeres testmozgás, egészséges étrend, és elegendő alvás enyhítheti. A dohányzás súlyosbíthatja a tüneteket, ezért ajánlott leszokni róla. 65 A széklettranszplantáció során egy egészséges személy székletét használják a beteg személy bélflórájának helyreállítására. Ez a terápiás megközelítés gyulladásos bélbetegségek, így Morbus Crohn esetén is egy működő, relatív kevés mellékhatással járó megközelítés. 69–70

Funkcionális orvoslás felőli megközelítés
Mint más autoimmun-betegségek integratív megközelítése esetén is, a Crohn-betegség funkcionális kezelésénél is a cél a gyulladás kiváltó okának feltárása és kezelése. Az integratív orvos ételintolerancia tesztet, székletvizsgálatot kérhet. Ezek segítségével, a beteggel együttműködve azonosíthatja a gyulladás kiváltó okát. Ilyen kiváltó, vagy súlyosbító okok lehetnek: bizonyos ételek, a bélflóra egyensúlyának zavara, baktériumok, gombák, paraziták, vírusok, áteresztő bél szindróma, vagy a nem megfelelő mennyiségű jótékony bélbaktérium. Az egyénre szabott, betegspecifikus teszt segítségével az integratív szemléletű szakember egy személyre szabott életmód- és étrendi tervet tud összeállítani, kihangsúlyozva a táplálkozás, a táplálékkiegészítők, a testmozgás, és adott esetben a meditáció fontosságát. 71 A Crohn-betegségben szenvedők számára ajánlott étrendek közé tartozik a specifikus szénhidrát-diéta (SCD) és az eliminációs diéta. Mindkét étrend a tüneteket kiváltó élelmiszerek eltávolítására, és helyette olyan egészséges ételek fogyasztására összpontosít, amelyek nem súlyosbítják a tüneteket. 71 Több étrendkiegészítő is hatékony lehet a Crohn-betegség kezelésére. Főleg gyulladáscsökkentők, mint az Omega 3 zsírsavak és a kurkuma alapú termékek. A cink-glicinát, az N-acetilglükózamin és a D3-vitamin pedig segíthet helyreállítani a bélflórát. 71
Dr. Lum's Plan for Crohn's & Ulcerative Colitis féle megközelítés
Az alábbiakban tárgyalt megközelítés nem helyettesíti az akut / sürgősségi kezelést. Dr. Lum megközelítése a Crohn-betegség okainak megszüntetésére és a gyógyulás támogatására szolgál 72: Ez a megközelítés egyaránt összpontosít a genetikai tényezőkre és a mögöttes fertőzések kezelésére. 1. lépés: az emésztés rendbetételeSósav: Fontos helyreállítani a gyomor természetes képességét a megfelelő mennyiségű sósav termelésére, hogy megkönnyítse az emésztést. Ehhez támogatni kell a gyomorsavat termelő szövetek és sejtek gyógyulását és regenerációját. Hasnyálmirigy-enzimek: Ezek az emésztőenzimek létfontosságúak az étel emésztéséhez és a felszívódáshoz. Az emésztőenzimek pótlása önmagában kevés - magát a hasnyálmirigyet is kezelni és gyógyítani kell. A cél, hogy az emésztés emésztőenzimek bevétele nélkül is működjön. Epe: Gyulladásos bélbetegségeknél gyakran zavart szenved az epe termelődése és áramlása is. Ennek egyik jele, ha valaki zsíros ételek után emésztési nehézségeket tapasztal. A megfelelő epeműködés elengedhetetlen a zsírok lebontásához és a zsírban oldódó vitaminok (A, E, K és D-vitamin) felszívódásához. Bélmozgás: Akár székrekedésről, akár hasmenésről van szó, a kezelés célja a bélmozgás egyensúlyának helyreállítása, hogy az emésztés se túl lassú, se túl gyors ne legyen. 2. lépés: a mikrobiom helyreállítása és a háttérben lévő fertőzések kezelése A mikrobiom közvetlenül befolyásolja a gyulladás súlyosságát, az immunrendszer egészségét és a teljes emésztést is. A bélflóra funkcionális elemzése a gyógyulás fontos tényezője. A lappangó fertőzések azonosítása és kezelése pedig a tartós tünetmentességhez elengedhetetlen. 3. lépés: genetikai hajlamok feltárása Egyes gének fokozhatják a gyulladásos folyamatokat, míg mások a szerotonin- és dopaminszint egyensúlyának felborulásához járulhatnak hozzá. Ezért fontos feltérképezni a genetikai hajlamokat, hogy célzottabban lehessen támogatni a szervezet egyensúlyának helyreállítását. 4. lépés: a májfunkció felmérése A gyulladásos bélbetegségekben szenvedők többségének mögöttes májproblémája van. A hagyományos vizsgálatok ugyanakkor nem elegendőek a májproblémák kizárásához. A beteg máj, beteg bélrendszert okozhat. A máj egészségének és működésének támogatása esetén a bélrendszer állapotának javulása gyorsabb lehet. Gyulladásos bélbetegségek esetén a szervezet megtámadja, és megpróbálja elpusztítani a káros mikrobákat, beleértve a vírusokat, baktériumokat, gombákat és parazitákat is. Az immunrendszernek ez a támadása okozza a gyulladásos bélbetegség esetén jelentkező krónikus gyulladást. Károsodott mikrobiom esetén a szervezet védelmi rendszere leáll, és egyre több fertőzés halmozódhat fel. Ezután az immunrendszer még erősebben próbálja elpusztítani a kórokozókat egyre több gyulladás kiváltásával. Ez az ördögi körforgás növeli a Crohn-betegség tüneteinek súlyosságát. A tünetek jelentkezése ciklikus jellegű, mivel különböző tényezők befolyásolják az immunrendszer egészségét, és a gyulladás súlyosságát. Az olyan tényezők, mint a tartós alváshiány, ételallergiák, feldolgozott élelmiszerek fogyasztása és a stressz súlyosbíthatják a tüneteket, és gyengíthetik az immunrendszer működését. Ezért a kezelés célja az immunrendszer erősítése a bélmikrobiom egyensúlyának helyreállításával, valamint a háttérben meghúzódó, rejtett fertőzések célzott kezelése. A megoldás A cél, hogy egyensúlyba hozzuk a szerotonin és dopamin neurotranszmittereket az agyban és a gyomor-bél rendszerben. A két neurotranszmitter kiegyensúlyozottsága esetén a túlzott szerotoninszint már nem váltja ki a gyulladásos folyamatot, így a bélszövet gyógyulni kezdhet. A kezelés része az orvos által irányított szerotonin- és dopamin-előanyagok (aminosav prekurzorok) pótlása. Emellett fontos szerepet kap a bélflóra egyensúlyának helyreállítása is, ami magában foglalja a fertőző kórokozók elpusztítását, a bélfal gyógyítását, valamint az immunrendszer megerősítését. A Crohn-betegség integratív megközelítés szempontjai közé tehát a megállapított táplálkozási hiányosságok lekűzdése, az ételek és tápanyagok asszimilációjának és emésztésének optimalizálása, a bélbaktériumok megfelelő számának és arányának elérése, egyénre szabott étrend kialakítása és a megfelelő bélflóra helyreállítása tartozik. A neurotranszmitter genetikai eltérések figyelembevétele a gyulladásos bélbetegségek tünetei enyhülésének egyik lehetséges tényezője. Egy másik, a funkcionális orvoslás felőli megközelítés, a Mullin’s DIGIN model 73. A DIGIN model a páciens egészségi állapotát öt alapvető területen vizsgálja, melyek az emésztés és felszívódás, a bél áteresztőképesség, a gyulladás, az immunrendszer, valamint az idegrendszer.
Egyéb összefüggések
Colitis ulcerosa
A Crohn-betegség tünetei hasonlóak a colitis ulcerosa, vagyis a fekélyes vastagbélgyulladás tüneteihez. Mindkettő gyulladásos bélbetegség, hasonló, a vastagbelet érintő tünetekkel. Fontos megkülönböztetni azonban a két megbetegedést, mivel lefolyásuk és kezelésük eltérő lehet. Azokban az esetekben amikor nem lehetséges különbséget tenni a két betegség között, a betegség meghatározatlan vastagbélgyulladásnak minősül. 3, 8–9 A Crohn-betegség a gyomor-bél traktus vastagbélen kívüli területeit is befolyásolhatja, a colitis ulcerosa viszont általában a vastagbélre korlátozódik 74. A colitis ulcerosa esetén a gyulladás a teljes érintett területen megtalálható, míg a Crohn-betegség esetében ez szakaszosan tapasztalható: párhuzamosan több helyen alakulhat ki a gyulladás, a gyulladt területek közt egészséges bélrészekkel.
IBD
Az IBD az inflammatory bowel disease, azaz magyarul a gyulladásos bélbetegség rövidítése. Az IBD egy betegségcsoportot jelent, ahova a Crohn-betegség és a colitis ulcerosa is tartozik. Egy 2014-es áttekintő kutatás szerint a Crohn-betegség súlyosabb, mint a colitis ulcerosa, ugyanakkor kevésbé gyakori. 75
IBS
Az irritábilis bél szindróma (IBS) nagyon gyakori betegség, a magyar lakosság 20%-át érinti. Az IBD-khez, így a Crohn-betegséghez hasonlóan, tünetei ciklikusan jelentkeznek. A fellángolások általában több napig tartanak és a panaszok étkezés után rosszabbak lehetnek. A nőknél a menstruáció időszakában több panasz jelentkezhet. 76 Az IBS általában a bélműködés hirtelen megváltozásával jár, például hasmenéssel vagy székrekedéssel. A tünetek az enyhétől a súlyosig változhatnak, és a következők lehetnek 76:
- hasmenés
- székrekedés
- hasfájás
- gyomorgörcsök
- gázképződés és puffadás
- hangos bélmozgás
- hiányos bélkiürítés érzése
- nyálkás széklet
Az IBD-k, mint a Crohn-betegség, és az IBS közötti hasonlóság, hogy mindkettő gyógyíthatatlan. Hasonló tüneteket okozhatnak, és diagnosztizálásuk is hosszadalmas folyamat. További hasonlóság, hogy az IBS és a Crohn-betegség is hosszú távú állapot, tüneteik váltakoznak a fellángolások, és a remissziók periódusai között. Mindkét betegség okozhat emésztőszerven kívüli panaszokat. 76 Különbség, hogy az IBD, amely magába foglalja a Crohn-betegséget, autoimmun betegség, míg az IBS valószínűleg emésztési problémákból és a bélflóra egyensúlyának felborulásából fakad. Az IBS élesen elkülönül a colitis ulcerosától és a Crohn-betegségtől abban a tekintetben is, hogy nem gyulladásos betegség. Az IBD-ben szenvedőknél gyógyszerek csökkenthetik a szimptómákat, míg az IBS kezelése elsősorban az életmódra és az étrend változására összpontosít. Mindezeken felül, az IBS, a Crohn-betegséggel ellentétben, jelenlegi tudásunk szerint, nem növeli a bélrák kialakulásának kockázatát. 71
A tünetei mögötti okokat keresi?
A funkcionális megközelítés segít megérteni, mi áll a panaszok hátterében — és személyre szabott tervet ad ahhoz, hogy újra jól érezze magát.
Konzultáció foglalásaTetszett a cikk? Iratkozz fel hírlevelünkre →
Források
79 forrásokForrások
[1] Mayo Clinic Staff, “Crohn’s disease - Symptoms and causes,” Mayo Clinic, 2020 https://www.mayoclinic.org/diseases-conditions/crohns-disease/symptoms-causes/syc-20353304
[2] M. Pimentel et al., “Identification of a prodromal period in Crohn’s disease but not ulcerative colitis,” Am. J. Gastroenterol., vol. 95, no. 12, pp. 3458–3462, 0 2000, DOI: https://doi.org/10.1111/j.1572-0241.2000.03361.x
[3] D. C. Baumgart and W. J. Sandborn, “Crohn’s disease,” Lancet Lond. Engl., vol. 380, no. 9853, pp. 1590–1605, 0 2012, DOI: https://doi.org/10.1016/S0140-6736(12)60026-9
[4] N. R. C. (US) C. on D. and C. of J. Disease, Johne’s Disease and Crohn’s Disease. National Academies Press (US), 2003 https://www.ncbi.nlm.nih.gov/books/NBK207651/
[5] Z. Risoldi Cochrane and K. Holland, “Crohn’s Disease: Causes, Symptoms, Diagnosis, and More,” Healthline, Aug. 22, 2018 https://www.healthline.com/health/crohns-disease
[6] “Crohn’s Disease | NIDDK,” National Institute of Diabetes and Digestive and Kidney Diseases https://www.niddk.nih.gov/health-information/digestive-diseases/crohns-disease/all-content
[7] M. H. Mueller, M. E. Kreis, M. L. Gross, H. D. Becker, T. T. Zittel, and E. C. Jehle, “Anorectal functional disorders in the absence of anorectal inflammation in patients with Crohn’s disease,” Br. J. Surg., vol. 89, no. 8, pp. 1027–1031, 0 2002, DOI: https://doi.org/10.1046/j.1365-2168.2002.02173.x
[8] D. K. Podolsky, “Inflammatory bowel disease,” N. Engl. J. Med., vol. 347, no. 6, pp. 417–429, 0 2002, DOI: https://doi.org/10.1056/NEJMra020831
[9] “Crohn Disease: Practice Essentials, Background, Pathophysiology,” Nov. 2019, https://emedicine.medscape.com/article/172940-overview
[10] Crohn’s & Colitis Foundation, “Overview of Crohn’s Disease,” Crohn’s & Colitis Foundation https://www.crohnscolitisfoundation.org/what-is-crohns-disease/overview
[11] M. Harbord et al., “The First European Evidence-based Consensus on Extra-intestinal Manifestations in Inflammatory Bowel Disease,” J. Crohns Colitis, vol. 10, no. 3, pp. 239–254, Mar. 2016, DOI: https://doi.org/10.1093/ecco-jcc/jjv213
[12] G. Trikudanathan, P. G. K. Venkatesh, and U. Navaneethan, “Diagnosis and therapeutic management of extra-intestinal manifestations of inflammatory bowel disease,” Drugs, vol. 72, no. 18, pp. 2333–2349, 0 2012, DOI: https://doi.org/10.2165/11638120-000000000-00000
[13] N. Roth et al., “Occurrence of skin manifestations in patients of the Swiss Inflammatory Bowel Disease Cohort Study,” PloS One, vol. 14, no. 1, p. e0210436, 2019, DOI: https://doi.org/10.1371/journal.pone.0210436
[14] B. Thrash, M. Patel, K. R. Shah, C. R. Boland, and A. Menter, “Cutaneous manifestations of gastrointestinal disease: part II,” J. Am. Acad. Dermatol., vol. 68, no. 2, p. 211.e1–33; quiz 244–246, Feb. 2013, DOI: https://doi.org/10.1016/j.jaad.2012.10.036
[15] “Crohn’s Disease : Epilepsy.com/Professionals,” Aug. 05, 2007 https://web.archive.org/web/20070805041654/http://professionals.epilepsy.com/page/inflammatory_crohn.html
[16] W. A. Bye, T. M. Nguyen, C. E. Parker, V. Jairath, and J. E. East, “Strategies for detecting colon cancer in patients with inflammatory bowel disease,” Cochrane Database Syst. Rev., vol. 9, p. CD000279, 18 2017, DOI: https://doi.org/10.1002/14651858.CD000279.pub4
[17] A. Ekbom, C. Helmick, M. Zack, and H. O. Adami, “Increased risk of large-bowel cancer in Crohn’s disease with colonic involvement,” Lancet Lond. Engl., vol. 336, no. 8711, pp. 357–359, 0 1990, DOI: https://doi.org/10.1016/0140-6736(90)91889-i
[18] K. Gerasimidis, P. McGrogan, and C. A. Edwards, “The aetiology and impact of malnutrition in paediatric inflammatory bowel disease,” J. Hum. Nutr. Diet. Off. J. Br. Diet. Assoc., vol. 24, no. 4, pp. 313–326, 0 2011, DOI: https://doi.org/10.1111/j.1365-277X.2011.01171.x
[19] M. C. E. Lomer, “Dietary and nutritional considerations for inflammatory bowel disease,” Proc. Nutr. Soc., vol. 70, no. 3, pp. 329–335, 0 2011, DOI: https://doi.org/10.1017/S0029665111000097
[20] J. H. Cho and S. R. Brant, “Recent insights into the genetics of inflammatory bowel disease,” Gastroenterology, vol. 140, no. 6, pp. 1704–1712, May 2011, DOI: https://doi.org/10.1053/j.gastro.2011.02.046
[21] R. Dessein, M. Chamaillard, and S. Danese, “Innate immunity in Crohn’s disease: the reverse side of the medal,” J. Clin. Gastroenterol., vol. 42 Suppl 3 Pt 1, pp. S144-147, Sep. 2008, DOI: https://doi.org/10.1097/MCG.0b013e3181662c90
[22] T. Stefanelli, A. Malesci, A. Repici, S. Vetrano, and S. Danese, “New insights into inflammatory bowel disease pathophysiology: paving the way for novel therapeutic targets,” Curr. Drug Targets, vol. 9, no. 5, pp. 413–418, May 2008, DOI: https://doi.org/10.2174/138945008784221170
[23] H. Braat, M. Peppelenbosch, and D. Hommes, “Immunology of Crohn’s Disease,” Ann. N. Y. Acad. Sci., 2006, DOI: https://doi.org/10.1196/annals.1326.039
[24] L. Henckaerts, C. Figueroa, S. Vermeire, and M. Sans, “The role of genetics in inflammatory bowel disease,” Curr. Drug Targets, vol. 9, no. 5, pp. 361–368, May 2008, DOI: https://doi.org/10.2174/138945008784221161
[25] J. C. Barrett et al., “Genome-wide association defines more than 30 distinct susceptibility loci for Crohn’s disease,” Nat. Genet., vol. 40, no. 8, pp. 955–962, 0 2008, DOI: https://doi.org/10.1038/ng.175
[26] M. Walker and J. A. Murray, “An update in the diagnosis of coeliac disease,” Histopathology, 2011, DOI: https://doi.org/10.1111/j.1365-2559.2010.03680.x
[27] A. Coghlan, “A single gene can either raise or lower Crohn’s disease risk,” New Scientist https://www.newscientist.com/article/single-gene-can-either-raise-lower-crohns-disease-risk/
[28] D. J. B. Marks and A. W. Segal, “Innate immunity in inflammatory bowel disease: a disease hypothesis,” J. Pathol., vol. 214, no. 2, pp. 260–266, 0 2008, DOI: https://doi.org/10.1002/path.2291
[29] D. J. B. Marks et al., “Defective acute inflammation in Crohn’s disease: a clinical investigation,” Lancet Lond. Engl., vol. 367, no. 9511, pp. 668–678, Feb. 2006, DOI: https://doi.org/10.1016/S0140-6736(06)68265-2
[30] G. M. Cobrin and M. T. Abreu, “Defects in mucosal immunity leading to Crohn’s disease,” Immunol. Rev., vol. 206, pp. 277–295, 0 2005, DOI: https://doi.org/10.1111/j.0105-2896.2005.00293.x
[31] C. O. Elson et al., “Monoclonal anti-interleukin 23 reverses active colitis in a T cell-mediated model in mice,” Gastroenterology, vol. 132, no. 7, pp. 2359–2370, Jun. 2007, DOI: https://doi.org/10.1053/j.gastro.2007.03.104
[32] M. Velasquez-Manoff, “The Worm Turns (Published 2008),” The New York Times, Jun. 29, 2008 https://www.nytimes.com/2008/06/29/magazine/29wwln-essay-t.html
[33] J. Carnahan, “3 Surprising Microbial Triggers of Crohn’s Disease,” Dec. 21, 2017 https://www.jillcarnahan.com/2017/12/20/3-surprising-microbial-triggers-crohns-disease/
[34] S. J. Ott et al., “Reduction in diversity of the colonic mucosa associated bacterial microflora in patients with active inflammatory bowel disease,” Gut, vol. 53, no. 5, pp. 685–693, May 2004, DOI: https://doi.org/10.1136/gut.2003.025403
[35] D. N. Frank, A. L. St. Amand, R. A. Feldman, E. C. Boedeker, N. Harpaz, and N. R. Pace, “Molecular-phylogenetic characterization of microbial community imbalances in human inflammatory bowel diseases,” Proc. Natl. Acad. Sci. U. S. A., vol. 104, no. 34, pp. 13780–13785, Aug. 2007, DOI: https://doi.org/10.1073/pnas.0706625104
[36] C. Manichanh et al., “Reduced diversity of faecal microbiota in Crohn’s disease revealed by a metagenomic approach,” Gut, vol. 55, no. 2, pp. 205–211, Feb. 2006, DOI: https://doi.org/10.1136/gut.2005.073817
[37] A. Darfeuille-Michaud et al., “High prevalence of adherent-invasive Escherichia coli associated with ileal mucosa in Crohn’s disease,” Gastroenterology, vol. 127, no. 2, pp. 412–421, 0 2004, DOI: https://doi.org/10.1053/j.gastro.2004.04.061
[38] K. Fetter et al., “The microbiome landscape in pediatric Crohn’s disease and therapeutic implications,” Gut Microbes, vol. 15, no. 2, p. 2247019, DOI: https://doi.org/10.1080/19490976.2023.2247019
[39] D.-Y. Kang et al., “Diagnosis of Crohn’s disease and ulcerative colitis using the microbiome,” BMC Microbiol., vol. 23, no. 1, p. 336, Nov. 2023, DOI: https://doi.org/10.1186/s12866-023-03084-5
[40] S. A. Naser, S. R. Sagramsingh, A. S. Naser, and S. Thanigachalam, “Mycobacterium avium subspecies paratuberculosis causes Crohn’s disease in some inflammatory bowel disease patients,” World J. Gastroenterol., vol. 20, no. 23, pp. 7403–7415, June 2014, DOI: https://doi.org/10.3748/wjg.v20.i23.7403
[41] S. A. Naser and M. T. Collins, “Debate on the lack of evidence of Mycobacterium avium subsp. paratuberculosis in Crohn’s disease,” Inflamm. Bowel Dis., vol. 11, no. 12, p. 1123, 0 2005, DOI: https://doi.org/10.1097/01.mib.0000191609.20713.ea
[42] G. Agrawal, T. J. Borody, and W. Chamberlin, “‘Global warming’ to Mycobacterium avium subspecies paratuberculosis,” Future Microbiol., vol. 9, no. 7, pp. 829–832, 2014, DOI: https://doi.org/10.2217/fmb.14.52
[43] W. Chamberlin, T. J. Borody, and J. Campbell, “Primary treatment of Crohn’s disease: combined antibiotics taking center stage,” Expert Rev. Clin. Immunol., vol. 7, no. 6, pp. 751–760, 0 2011, DOI: https://doi.org/10.1586/eci.11.43
[44] M. L. Scribano and C. Prantera, “Use of antibiotics in the treatment of Crohn’s disease,” World J. Gastroenterol., vol. 19, no. 5, pp. 648–653, Feb. 2013, DOI: https://doi.org/10.3748/wjg.v19.i5.648
[45] M. Baumgart et al., “Culture independent analysis of ileal mucosa reveals a selective increase in invasive Escherichia coli of novel phylogeny relative to depletion of Clostridiales in Crohn’s disease involving the ileum,” ISME J., vol. 1, no. 5, pp. 403–418, Sept. 2007, DOI: https://doi.org/10.1038/ismej.2007.52
[46] M. Sasaki et al., “Invasive Escherichia coli are a feature of Crohn’s disease,” Lab. Investig. J. Tech. Methods Pathol., vol. 87, no. 10, pp. 1042–1054, Oct. 2007, DOI: https://doi.org/10.1038/labinvest.3700661
[47] M. Martinez-Medina et al., “Biofilm formation as a novel phenotypic feature of adherent-invasive Escherichia coli (AIEC),” BMC Microbiol., vol. 9, p. 202, Sept. 2009, DOI: https://doi.org/10.1186/1471-2180-9-202
[48] K. P. Nickerson and C. McDonald, “Crohn’s disease-associated adherent-invasive Escherichia coli adhesion is enhanced by exposure to the ubiquitous dietary polysaccharide maltodextrin,” PloS One, vol. 7, no. 12, p. e52132, 2012, DOI: https://doi.org/10.1371/journal.pone.0052132
[49] H. Yanai, N. Shimizu, S. Nagasaki, N. Mitani, and K. Okita, “Epstein-Barr virus infection of the colon with inflammatory bowel disease,” Am. J. Gastroenterol., vol. 94, no. 6, pp. 1582–1586, June 1999, DOI: https://doi.org/10.1111/j.1572-0241.1999.01148.x
[50] J. L. Ryan et al., “Epstein-Barr virus infection is common in inflamed gastrointestinal mucosa,” Dig. Dis. Sci., vol. 57, no. 7, pp. 1887–1898, July 2012, DOI: https://doi.org/10.1007/s10620-012-2116-5
[51] S. Lapsia, S. Koganti, S. Spadaro, R. Rajapakse, A. Chawla, and S. Bhaduri-McIntosh, “Anti-TNFα therapy for inflammatory bowel diseases is associated with Epstein-Barr virus lytic activation,” J. Med. Virol., vol. 88, no. 2, pp. 312–318, Feb. 2016, DOI: https://doi.org/10.1002/jmv.24331
[52] R. Ciccocioppo et al., “Human cytomegalovirus and Epstein-Barr virus infection in inflammatory bowel disease: need for mucosal viral load measurement,” World J. Gastroenterol., vol. 21, no. 6, pp. 1915–1926, Feb. 2015, DOI: https://doi.org/10.3748/wjg.v21.i6.1915
[53] B. H. Mullish and H. R. Williams, “Clostridium difficile infection and antibiotic-associated diarrhoea,” Clin. Med., vol. 18, no. 3, pp. 237–241, June 2018, DOI: https://doi.org/10.7861/clinmedicine.18-3-237
[54] L. Saidel-Odes, A. Borer, and S. Odes, “Clostridium difficile infection in patients with inflammatory bowel disease,” Ann. Gastroenterol. Q. Publ. Hell. Soc. Gastroenterol., vol. 24, no. 4, pp. 263–270, 2011 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC6334067/
[55] B. G. Mitchell and A. Gardner, “Mortality and Clostridium difficile infection: a review,” Antimicrob. Resist. Infect. Control, vol. 1, p. 20, May 2012, DOI: https://doi.org/10.1186/2047-2994-1-20
[56] N. T. Shen et al., “Timely Use of Probiotics in Hospitalized Adults Prevents Clostridium difficile Infection: A Systematic Review With Meta-Regression Analysis,” Gastroenterology, vol. 152, no. 8, pp. 1889-1900.e9, June 2017, DOI: https://doi.org/10.1053/j.gastro.2017.02.003
[57] J. Burisch and P. Munkholm, “Inflammatory bowel disease epidemiology,” Curr. Opin. Gastroenterol., 2013, DOI: https://doi.org/10.1097/MOG.0b013e32836229fb
[58] N. A. Molodecky et al., “Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review.,” Gastroenterology, 2012, DOI: https://doi.org/10.1053/j.gastro.2011.10.001
[59] Ø. Hovde and B. A. Moum, “Epidemiology and clinical course of Crohn’s disease: results from observational studies,” World J. Gastroenterol., vol. 18, no. 15, pp. 1723–1731, Apr. 2012, DOI: https://doi.org/10.3748/wjg.v18.i15.1723
[60] “Crohn’s Disease Symptoms, Diet, Pictures, Drugs, Life Expectancy,” eMedicineHealth https://www.emedicinehealth.com/crohn_disease/article_em.htm
[61] R. Shoda, K. Matsueda, S. Yamato, and N. Umeda, “Epidemiologic analysis of Crohn disease in Japan: increased dietary intake of n-6 polyunsaturated fatty acids and animal protein relates to the increased incidence of Crohn disease in Japan,” Am. J. Clin. Nutr., vol. 63, no. 5, pp. 741–745, May 1996, DOI: https://doi.org/10.1093/ajcn/63.5.741
[62] J. Cosnes, “Tobacco and IBD: relevance in the understanding of disease mechanisms and clinical practice,” Best Pract. Res. Clin. Gastroenterol., vol. 18, no. 3, pp. 481–496, June 2004, DOI: https://doi.org/10.1016/j.bpg.2003.12.003
[63] S. M. Lesko et al., “Evidence for an increased risk of Crohn’s disease in oral contraceptive users,” Gastroenterology, vol. 89, no. 5, pp. 1046–1049, 0 1985, DOI: https://doi.org/10.1016/0016-5085(85)90207-0
[64] F. Shanahan, “Crohn’s disease,” Lancet Lond. Engl., vol. 359, no. 9300, pp. 62–69, 0 2002, DOI: https://doi.org/10.1016/S0140-6736(02)07284-7
[65] J. K. Hou, B. Abraham, and H. El-Serag, “Dietary intake and risk of developing inflammatory bowel disease: a systematic review of the literature,” Am. J. Gastroenterol., vol. 106, no. 4, pp. 563–573, Apr. 2011, DOI: https://doi.org/10.1038/ajg.2011.44
[66] M. Khatri, “Crohn’s Disease,” WebMD https://www.webmd.com/ibd-crohns-disease/crohns-disease/digestive-diseases-crohns-disease
[67] S. B. Hanauer, “Inflammatory bowel disease,” N. Engl. J. Med., vol. 334, no. 13, pp. 841–848, Mar. 1996, DOI: https://doi.org/10.1056/NEJM199603283341307
[68] “Inflammatory bowel disease (IBD) - Diagnosis and treatment - Mayo Clinic” https://www.mayoclinic.org/diseases-conditions/inflammatory-bowel-disease/diagnosis-treatment/drc-20353320
[69] S. R. Jeon, J. Chai, C. Kim, and C. H. Lee, “Current Evidence for the Management of Inflammatory Bowel Diseases Using Fecal Microbiota Transplantation,” Curr. Infect. Dis. Rep., vol. 20, no. 8, p. 21, May 2018, DOI: https://doi.org/10.1007/s11908-018-0627-8
[70] A. N. Levy and J. R. Allegretti, “Insights into the role of fecal microbiota transplantation for the treatment of inflammatory bowel disease,” Ther. Adv. Gastroenterol., vol. 12, Mar. 2019, DOI: https://doi.org/10.1177/1756284819836893
[71] C. Abercrombie, L. Houser, and G. Tetlow, “An Integrative Approach to Crohn’s Disease: Exploring Autoimmunity in the Gut. You and your Healthy Belly- Part 3,” Philadelphia Integrative Medicine, 2016 https://philly-im.com/blog/integrative-approach-crohns-disease-exploring-autoimmunity-gut-healthy-belly-part-3
[72] B. Dr. Lum, “Functional Medicine For Crohn’s & Ulcerative Colitis | Dr. Brian Lum,” drbrianlum, 2020 https://www.drbrianlum.com/crohn-s-ulcerative-colitis
[73] K. Schepker, “To Help Patients with Irritable Bowel, Clinicians Need to ‘DIGIN,’” Holistic Primary Care, Aug. 13, 2018 https://holisticprimarycare.net/topics/chronic-disease/a-functional-medicine-approach-to-ibd-treatment/
[74] D. T. Rubin, A. N. Ananthakrishnan, C. A. Siegel, B. G. Sauer, and M. D. Long, “ACG Clinical Guideline: Ulcerative Colitis in Adults,” Am. J. Gastroenterol., vol. 114, no. 3, pp. 384–413, 2019, DOI: https://doi.org/10.14309/ajg.0000000000000152
[75] K. Gohil and B. Carramusa, “Ulcerative Colitis and Crohn’s Disease,” Pharm. Ther., vol. 39, no. 8, pp. 576–577, Aug. 2014 https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4123809/
[76] “IBD vs. Crohn’s disease vs. IBS: Symptoms, diagnosis, and treatment,” Nov. 22, 2018 https://www.medicalnewstoday.com/articles/323778