Mitokondriumok működése, funkciói, diszfunkciói, helyreállítása

A mitokondriumok eredete
A mitokondriumok az általánosan elfogadott elképzelés, az ún. endoszimbionta elmélet szerint egykor önálló baktériumok voltak, melyeket kb. egy milliárd évvel ezelőtt archeobaktériumok kebeleztek be. Egy sejt egy másik sejt általi bekebelezése (fagocitózis) egysejtűek köreiben a táplálkozásnak egy viszonylag szokványos módja, immunrendszerünk egy része is így bánik el a kórokozókkal, a bekebelezett sejt megemésztődik. Ebben az esetben viszont a megemésztés helyett a két sejt együttműködni kezdett, és az így kialakult szimbiózis olyan sikeres lett, hogy a teljes fejlett élet erre a folyamatra vezethető vissza. A mitokondriumok a mai napig a baktériumokra jellemző kettős sejtfallal rendelkeznek, és saját DNS-sel is. Sejtjeinkben részben szexuálisan, részben osztódással szaporodnak, ill. sejtjeinken kívül is képesek létezni, közlekedni. A mitokondriumok bakteriális tulajdonságait ismerve érthetővé válnak az egészség krónikus károsodásának egyes útvonalai. A mitokondriumokat károsítani tudják krónikus fertőzéses, gyulladásos állapotok, mert ilyenkor a szervezet saját maga a baktériumokra nézve toxikus anyagokat termel. Egyes gyógyszerhatóanyagok is károsíthatják a mitokondriumok metabolizmusát, pl. egyes antibiotikumok, főleg gyakoribb, vagy hosszabb alkalmazás esetén, hiszen ezek a hatóanyagok a baktériumok metabolizmusát veszik célba, és így a mitokondriumok is megsérülhetnek.
A mitokondriumok funkciói
A mitokondriumok fontosabb funkciói:
- ATP, a szervezet energiahordozó molekulájának termelése cukorból, fehérjéből és zsírból
- Pregnenolon, az összes szteroid hormon (kortizol, progeszteron, ösztrogén, tesztoszteron, aldoszteron és egyebek) előanyagának termelése
- Hem szintézis (a hemoglobin alapja)
- Apoptózis (programozott sejthalál): A sejtek differenciálódásának, így az embrionális fejlődésnek, és az immunrendszer működésének is az alapja
- Cukor (glükóz) szintézis a vércukor stabilizálására (hiányában vércukor esések)

A mitokondriumok sejtjeink apró erőművei. Kb. 1- 5 mcm nagyságú sejtszervecskék, melyek száma sejtenként eltérő annak függvényében, hogy mekkora az adott sejttípus energiaigénye. Mitokondriumokban a leggazdagabbak az idegsejtek, amik kb. 10 000, a petesejt akár 100 000 mitokondriumot is tartalmazhat. A szív teljes súlyának pedig 36%-át a mitokondriumok teszik ki. A trombocitákban csak 2-6 db mitokondrium van, egyedül az érett eritrocitákban nincs egy sem. Szervezetünk energiájának 95%-át a mitokondriumok termelik ATP formájában. Egy egészséges személy átlagosan naponta 3000-szer alakítja az ADP-t ATP-vé, ami kilogrammban kifejezve 70 kg. Ha ez a rendszer nem működik megfelelően, energiahiány lép fel, ami a szervezet legkülönbözőbb szervrendszereit érintheti.

A mitokondriumok felépítése
A mitokondriumokat kettős membrán veszi körül. A külső relatív sima membrán viszonylag jól átereszti az ionokat és egyes kisebb molekulákat, mint pl. cukrokat. Csatornácskákat (porinok) tartalmaz, amik egyes fehérjék közlekedését teszik lehetővé a citoszol (sejtplazma) és a két mitokondriális membrán közötti tér között. A belső membrán erősen redőzött, ezáltal óriási a felülete van, ami a membránba épült energiatermelő folyamatok lezajlásának helyszíne. A belső membrán 70%-ban fehérjéből, 30%-ban foszfolipidekből áll, foszfatidilkolin (=lecitin) és szerinből, etanolaminból, difoszfatidilglicerolból (=kardiolipin) és foszfatidilinozitolból. Ezek a foszfolipidek nagy mennyiségű telítetlen zsírsavat is tartalmaznak, pl. DHA-t. A belső membrán, ha ép, kizárólag víz és egyes gázok számára átjárható, egyéb anyagokat egy sor transzport protein szállít. A belső membránba beágyazva találhatóak a légzési lánc (terminális oxidáció) fehérjekomplexei, 4 egybeépített komplex, és egy ötödik, egy miniatűr, a saját tengelye körül szélsebesen forgó miniatűr biomotor, ami az ATP-t szintetizálja.A belső membrán által bezárt térben, amit mátrixnak neveznek, találhatóak a citrátkör enzimei, és a mitokondriális DNS, ami baktériumokra jellemző módon gyűrű alakú, 37 génből áll, a mitokondrium génkészletének 15%-át kódolja. A mitokondrium többi génje a sejtmagban tárolódik. A mitokondriális DNS más felépítésű, mint a sejtmag DNS-e, nem tartalmaz hisztonokat (A DNS-t tömörítő, szabályzó, védő fehérje), így viszonylag sérülékeny. Mutációk gyakran érintik ezt a DNS-t, ez a probléma az életkorral, életmód hibákkal növekszik. A mitokondriumok anyai ágon öröklődnek, a hímivarsejtek csak a farok részben tartalmazzák őket, amik leválnak megtermékenyítéskor. Mivel a mitokondriális DNS egy része a sejtmagban van, mitokondriális gének, így génhibák hibák apai ágon is öröklődhetnek. A mitokondriumban található gének több példányban vannak jelen, ha ezek egy része megsérül, a többi ideig-óráig kompenzálni tudja a hibát.

Becslések szerint a hibák 20% kompenzálható. 40% esetén az érintettek a teherbíró képességük csökkenéséről számolnak be, csökkent alkohol toleranciáról, testsúlynövekedésről. 60% körüli küszöb értéknél jelennek meg klinikai tünetek, ami súlyos krónikus fáradtságot, kimerültséget jelent, az energia ekkor csak a létfontosságú szervek működtetéséhez elég. A károsodás hátterében krónikus fertőzések, toxikus hatások, stressz, túlterheltség, tápanyaghiányok, gyógyszerek, oltások állhatnak.
Mitokondriális diszfunkciók, mitokondriopátiák
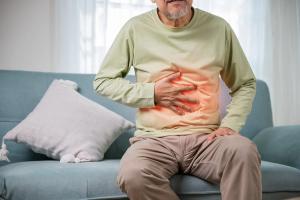
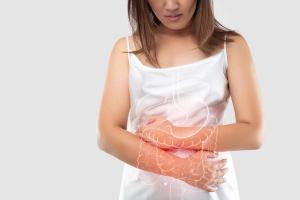
A mitokondriális funkciózavarok biokémiailag, genetikailag, és klinikailag is heterogének, a zavarok spektruma felnőtt korban megjelenő enyhe, egy-egy szervet érintő zavartól a legsúlyosabb, több szervrendszert érintő gyermekkori betegségekig (pl. Leigh-szindróma) terjedhet. Enyhébb esetekben mitokondriális diszfunkciókról beszéltünk, ezek gyakran bizonyos fokig reverzibilisek, tehát megfelelő terápiás megközelítésekkel, életmód protokollokkal visszafordíthatóak. Súlyos veleszületett, vagy szerzett formák esetén mitokondriopátiákról beszélünk. Megkülönböztetünk primer (veleszületett) és szekunder (az élet során kialakult) zavarokat. Primer mitokondriopátiáknál súlyos örökletes zavarokról beszélünk. Szekunder (szerzett) mitokondriopátiák, vagy mitokondriális diszfunkciók esetén olyan a mitokondriális DNS-t is érintő sérülésekről van szó, amelyek az egyén élete során alakultak ki. Ezeknek okai lehetnek a mitokondriumok működéséhez szükséges tápanyagok hiányai, ún. nitrozatív és oxidatív stressz (gyakran krónikus infekcióval a háttérben), vagy egyes a mitokondriumokra nézve toxikus gyógyszerhatóanyagok használata. Ezek a zavarok bármely életkorban felléphetnek, és bármely szerv működését érinthetik, de jellemzően olyan energia- és oxigénigényes szervek érintettek, mint az agy, szívizom, endokrin szervek, vérképző rendszer, máj, vese, ideg- és izomrendszer, és az érzékszervek, a legsérülékenyebb a retina. A mitokondriumok szerzett zavarai is főleg, de nem kizárólag anyai ágon öröklődnek. A mitokondriális működés összeomlása összességében energiahiányos, szteroid hormonhiányos, immunhiányos, különböző típusú ingerekre túlérzékeny állapotokat hoz létre, ill. vércukoresések, inzulinrezisztencia, bélfaldiszfunkciók, pszichés, pszichiátriai és neurológiai problémák, szívizomgyengeség, ill. a masztocita aktiváció / hisztamin intolerancia is hátterében is állhat, de még onkológiai problémák mögött is. (A mitokondriumok által generált apoptózis, a programozott sejthalál szükséges az immunsejtek differenciálódásához, és akadályozza meg a sérült sejtek túlélését, és fék nélküli burjánzását is.)
A mitokondriális diszfunkciók okai és tünetei
Különböző anyagcsere folyamatok során természetes módon termelődnek ún. szabad gyökök, melyeket 2 csoportba sorolunk, reaktív oxigéngyökök (ROS) és reaktív nitrogén gyökök (RNS). Ezeket a gyököket részben a szervezett “beépített” antioxidáns rendszerei semlegesítik, részben az étrendi antioxidáns tápanyagok, vitaminok. Az egyensúlyt megboríthatja egy krónikus infekcióra, környezeti mérgekre, nehézfémekre, gyógyszerhatóanyagokra, és/vagy krónikus stresszre adott válaszként megjelenő megnövekedett szabadgyök termelődés, vagy a szervezet antioxidáns kapacitásának a csökkenése. A szabadgyökök nagyon reakcióképes vegyületek, toxikus anyagcseretermékek (pl. peroxinitrit) képződéséhez járulnak hozzá. Ezek az anyagok a viszonylag védetlen mitokondriális DNS sérülésének veszélyével járnak. A szabadgyökök egyes enzimeket is gátolnak, ezen kívül a belső mitokondriális membrán áteresztését is fokozzák. Ezek a folyamatok összességében a sejtszintű energia termelésének csökkenését okozzák, aminek a tünetei lehetnek kimerülés, levertség, motiválatlanság. Mitokondriális diszfunkciók a következő zavarok esetében állhatnak akár okilag, akár kísérő problémaként:
- Krónikus fáradtság szindróma (CFS)
- Burnout
- Depresszív hangulat
- Neurodegeneratív megbetegedések (M. Alzheimer, M. Parkinson)
- Koncentrációs zavarok
- Inzulin rezisztencia
- Metabolikus szindróma (Diabétesz, magas vérnyomás, elhízás)
- Szív- érrendszeri megbetegedések
- Szteriod hormon hiányok, hisztamin intolerancia
- Az immunrendszer működésének zavarai

Az egyes szervrendszereket érintő mitokondriopátiák súlyos klinikai következményei (Uwe Gröber):
| Érintett szerv | Következmények |
|---|---|
| Máj | Májelégtelenség, mikroveszikuláris szteatózis, nem-alkoholos steatohepatitisz |
| Vese | Tubulopátiák, Fanconi-szindróma, nefrotikus szindróma |
| Szívizom | Dilatív, vagy hipertróf kardiomiopátia, szívelégtelenség, Barth-szindróma |
| Érzékszervek Szem Fül Orr | Retinopátiák, látóideg atrófia, ptózis (lógó szemhéj), szemizombénulás, nystagmus Hallásvesztés, tinnitusz Anozmia (szaglás elvesztése) |
| Vázizomzat | Mioklóniák, izomfájdalmak, rhabdomiolízis, muszkuláris hipotónia |
| Endokrin szervek | Endokrin-metabolikus megbetegedések: Diabetes mellitus, pajzsmirigy alulműködés, mellékpajzsmirigy alulműködés |
| Idegrendszer, agy | Neurpoátiák, ataxia (mozgások lezajlásának zavarai), központi idegrendszerből kiinduló görcsrohamok |

Mitokondrium - digitális illusztráció
Egyes gyógyszerhatóanyagok a mitokondriális diszfunkciók hátterében
A gyógyszerhatóanyagok által kiváltott ún. mitokondriális toxicitás mechanizmusai különbözőek. Egy részük a sérülékeny mitokondriális membránokat, más részük a sokféle elemi fontosságú biokémiai mechanizmusok valamelyikét károsítja. Az USA-ban egyes becslések szerint az akut májkárosodást okozó gyógyszerek több, mint a fele, és gyógyszerek piacról való levételének többségének a hátterében mitokondriális károsodás okozása áll. A gyógyszerhatóanyagok mitokondriumokat károsító hatásai a következő területeken történnek (Uwe Gröber):
| Mechanizmus | Hatóanyagok, hatóanyagcsoportok |
|---|---|
| A légzési lánc enzimek gátlása | Simvastatin (koleszterin szint csökkentő) Metformin (orális antidiabetikum) Amoidaron (szívritmusszabályzás) Haloperidol (neuroleptikum) |
| Az oxidatív foszforiláció szétkapcsolása | Ibuprofen, diclofenac (NSAID) Tamoxifen (antiösztrogén) |
| A béta-oxidáció gátlása | Tetraciklinek (antibiotikumok) Tamoxifen (antiösztrogén) |
| Lipidperoxidáció és glutation depléció | Epirubicin, Cisplatin (citosztatikumok) Valproinsav (antiepileptikum) |
| Mitokondriális DNS depléció | Paracetamol (fájdalomcsillapító) |
| A membrán-permeabilitás és integritás megzavarása | Epirubicin, Doxorubicin (citosztatikumok) |
Egyes gyakran felírt gyógyszerhatóanyagok a következő úton okoznak mitokondriális diszfunkciókat:
Metformin (Biguanidok)
A metformin orális antidiabetikum a bazális és étkezés utáni vércukorszint csökkentésére. A biguanidok farmakológiai hatása a májban létrejövő glukoneogenezis és glükogenolízis gátlása, és az izomsejtek inzulinérzékenységének a fokozása, amivel a cukor perifériás felvétele és hasznosulása javul. A biguanoidok komplex hatásmechanizmusának a része a mitokondriális légzési láncba való beavatkozás (I-es komplex), ami miatt súlyos mellékhatások léphetnek fel. Ezek között vannak emésztőrendszeri tünetek: Hasi fájdalmak, hasmenés, hányinger, hányás. Több biguanid hatóanyagot (buformin, fenformin) szív-érrendszeri mellékhatások, és életveszélyes laktoacidózisok előfordulása miatt levettek a piacról. Ezek a metforminnál kb. 20 x gyakrabban okoztak laktoacidózist, de ez ritkán ugyan, de metformin esetében is előfordul. A mitokondriális légzési lánc I-es komplexének a gátlása a biguanoidok által azt eredményezi, hogy a mitokondriális ATP termelés csökken, így a sejt kénytelen a kevésbé hatékony glükolízisből energiát nyerni, ami során több cukrot bont ugyan, de a folyamat eredményeként tejsav halmozódik fel a sejtekben. Ez különösen problémás olyan betegek esetén, akiknek a máj- és vesefunkciója korlátozott, mert náluk a hatóanyag kevésbé ürül a szervezetből. Egy másik magasabb rizikójú csoportot azok a betegek képezik, akiknél gyakran lép fel szöveti hipoxia, pl. szívelégtelenség, tüdőembólia infarktus vagy sokkos állapot miatt. A metformin ritkán okoz laktacidózist, amikor viszont igen, a tünetek lassan, nem specifikus módon kezdődnek, hasfájással, hányingerrel, fáradtsággal, nyugtalansággal, légszomjjal és keringési zavarokkal, az orvosi kezelés emiatt későn kezdődik, az esetek közel fele emiatt halállal végződik. A metformin rendszeres alkalmazásának másik negatív következménye a B12-vitamin felvételét a leválasztásához és felszívódásához szükséges Intrinsic Factor gátlásán keresztül. A folsav és B12-vitamin a metiláció támogatásán keresztül is a megfelelő mitokondriális működés fenntartásához is szükséges, ezen kívül a B12-vitaminnak a citrátkör (Krebs-ciklus) fenntartásában is szerepe van. A citrátkör az a biokémiai reakciólánc, ami a közös útvonal a szénhidrátok, aminosavak, és lipidek energiává alakításában. A B12 hiány tünetei krónikus fáradtságon, és makrociter anémián kívül gyakran nyilvánul meg a legkülönbözőbb neurológiai zavarokban, neuropátiákban, depressziótól demenciákig terjedő módon. A B12-vitamin mérése csalóka, a Metilmalonsav (MMA) és homocisztein mérés is javasolt, ill. a laktát/piruvát arány vérből a szénhidrát hasznosulás ellenőrzésére. A B12-vitamin metilkobalamin formában való pótlása mellett az alfa-liponsav, Q10 vitamin és B1-vitamin (leginkább benfotiamin formában), ill. taurin és magnézium, ill. egyéb mitokondriális hatóanyagok pótlásával lehet a diabétesz, ill. a metformin szedés következményeit csökkenteni.
Sztatinok (CSE-gátlók)
A sztatinok koleszterinszint csökkentő hatóanyagok a szív-érrendszeri megbetegedések megelőzésére, világszerte a leggyakrabban felírt gyógyszerhatóanyag csoportok egyike. A sztatinok sajnos nemcsak a koleszterin szintézist gátolják, hanem más, ún. Izopentenilpirofoszfátot felépítő biomolekula szintézisét is, így a Q10 vitaminét is. Ennek a hatóanyagcsoportnak az egyik legproblémásabb mellékhatása a vázizomzatot érinti, és enyhe izomgyengeségtől életveszélyes rabdomiolízisig terjed. (A mellékhatás miatt 2001-ben piacról levett Cervistatin világszerte 52 regisztrált halálesetet okozott.) A sztatinok által okozott izomkárosodás hátterében megzavart mitokondriális funkciók egész sora áll: A már említett Q10 vitamin szintézisének a gátlásán túl a sztatinok a mitokondriális légzési lánc több komplexét is közvetlenül gátolják (egyes sztatinok különböző komplexeket gátolnak (pl. a simvastatin az összeset, a parvastatin pedig alig érinti ezeket), ezen kívül az elektronok transzportját is, és az oxidatív foszforilációt, a hem szintézist és károsítják a mitokondriális DNS-t is. A sztatinok diabetogén hatására hívta fel a figyelmet egy 2010-ben nyilvánosságra került kutatás, 4 évig követték a több, mint 90 000 vizsgált személyt, azok, akik sztatin terápiában részesültek, 9%-al nagyobb valószínűséggel lettek cukorbetegek. A mechanizmus molekuláris háttere egyelőre nem teljesen tisztázott, nem kizárt a mitokondriumok érintettsége. HIV
Paracetamol
A paracetamol világszerte az egyike a leggyakrabban felírt fájdalom-, és gyulladáscsökkentő hatóanyagoknak. Mindeközben ez a hatóanyag felel a leggyakrabban az akut májelégtelenség eseteiért. Csak az USA-ban évente több, mint 100 000 mérgezés történik, és akár 500 haláleset is. A paracetamol májkárosító hatásáért a citokróm p450 rendszer keretei között létrejövő N-acetil-p-benzochinonimin nevű magasan reaktív paracetamol-metabolit, amit általában a glutation semlegesít, de ha ebből nem áll elegendő rendelkezésre, vagy a glutation-transzferáz enzim kapacitásának a határához ér, a májsejtek végleges károsodást szenvedhetnek el. A paracetamol által kiváltott májkárosodás hátterében a májsejtek mitokondriumainak N-acetil-p-benzochinonimin általi funkcionális és morfológiai károsítása áll. HIV Ez a vegyület erősen kötődik a mitokondriumok fehérjéihez, és a máj mitokondriumainak oxidatív és nitrozatív gyökökkel való fokozott terhelését váltja ki. Emiatt a mitokondriumokban rendelkezésre álló glutation szint csökken, és a mitokondriális membrán megségül, áteresztővé válik kis molekulák számára, majd feloldódik, és apoptózist indukáló folyamatok kapcsolnak be, és a mitokondriális DNS is szétesik. Fontos: Paracetamol mérgezés esetén N-acetilcisztein adásával a mitokondriális glutation tartalékok feltöltődnek, ill. a toxikus paracetamol-metabolitok is semlegesíthetőek. Ha a terápia időben megkezdődik, a végzetes kimenetelű májpusztulás és májelégtelenség megállítható.
Valproinsav
A valproinsav egy széles hatású epilepszia ellenes gyógyszerhatóanyag. Leggyakrabban primer generalizált, ill. Fokális epilepsziák, de esetenként bipoláris, ill. mániás állapotokban használják. A valproinsavval való terápia is képes reverzibilis, vagy akár irreverzibilis májkárosodást kiváltani. Ezeknek az állapotoknak a kezdeti tünetei nem túl specifikusak, étvágytalanság, hányinger, hányás, fáradtság, letargia, gyengeség érzése, hasfájás, kék foltok megjelenése, és orrvérzés. Halálos kimenetelű eseteket leginkább két éven aluli gyermekek esetében írtak le. A valproinsav terápiát, főleg csecsemők, vagy kisgyerekek esetén a máj állapotának a folyamatos figyelemmel kísérése mellett javasolt folytatni. A valproinsav egy elágazó láncú zsírsav, a májban más gyógyszerhatóanyagokhoz hasonlóan glükuronidáció, vagy oxidáció útján, citokróm-p450 enzimek részvételével bomlik, zsírsavént bekerülhet a mitokondriumokba, hogy a béta-oxidáció útjára lépjen. Ennek során 20 különböző metabolit tud keletkezni
Célzott táplálékkiegészítéssel a mellékhatások semlegesítésére
A minimum, amit a gyógyszerhatóanyagok károsító hatásának a csökkentésére, megelőzésére tehetünk, azon kívül, hogy átgondoljuk, valóban szükség van-e ezeknek a hatóanyagoknak a használatára és hogy . van-e lehetőség alacsonyabb dózisra, az a párhuzamosan adott magasabb adagolású Q10 és L-karnitin adagolás, ill. egyéb mitokondriális vitaminok, és ásványi anyagok pótlása. Mindezekkel a gyógyszermellékhatások egy része kiküszöbölhető, sőt, sok esetben a gyógyszerhatóanyag vagy alacsonyabb dózisban is elegendően hat, vagy egyenesen okafogyottá válik.
A mitokondriális működés támogatásának lehetőségei
A mitokondriumok támogatása mindig jót tesz a szervezetnek, de nagyon különbözik a megközelítés, ha egészséges mitokondriumok működését akarjuk javítani, vagy betegeket regenerálni. Ami az egészséges embert edzi, az a betegekben további károkat okoz. Testmozgás mitokondriális problémák esetén (akár laborral igazolt, akár az energiahiány súlyossága miatt feltételezett esetben), óvatosan javasolt. Ha ugyanis a mitokondriumok energiatermelő kapacitása már megsérült, a sejt tejsavas erjedéssel próbál energiát nyerni, így a citoplazmában tejsav szaporodik fel. A hirtelen megnőtt savszint blokkolhatja a mitokondriális működést, súlyos fáradtságot okozva akár a testmozgást követő 24-48 órára is. A mozgásmennyiséget lassan szabad csak növelni, ne jelenjen meg a súlyos fáradtság. Jól működnek a következők: hidegterápia, szaunázás, oxigénterápia, infravörös sugarak, infralámpa. Már kialakult diszfunkció esetén nem javasolt a szénhidrát- és kalória csökkentett étrend sem. Javasolt a gyakori étkezés, ami fehérje és egészséges zsiradék mellett valamennyi komplex szénhidrátot (keményítőt) is tartalmazzon, hangsúlyosabban a délutáni/esti étkezés során. Böjtölni csak óvatosan javasolt, a leeső vércukor komoly stresszt jelent a szervezet számára. Az energiaszint javulásával, és ha nincsenek vércukor esések, nyújthatóak az étkezések közötti időszakok. Zsíros húsok, pl. egy-egy szelet lágy steak egyszerre biológiailag hasznosuló vas, zsír- és karnitin (és Q10) források, a karnitin juttatja a zsírt a membránon keresztül, ez javítja a bélfal és immunfunkciókat, és a mitokondriális energiatermelést is. A vasra az oxigén szállításához van szükség, a szervezet legfőbb oxigént használó rendszere a mitokondriális energiatermelés. Az energiahiány miatt szénhidrátéhség állhat fenn, viszont a mitokondriumok nem tudnak egyszerre nagyobb mennyiségű cukrot felvenni, így nagyobb mennyiségű szénhidrát fogyasztása esetén a sejtekben tejsav keletkezik, ami súlyos fáradtsághoz vezet. Eleinte napi 5 alkalommal kisebb adag vegyes, színes, fehérjében, egészséges zsírokban és másodIagos növényi hatóanyagokban is gazdag étrend. A mitokondriumban zajlik a sejtlégzés, az oxidáció. Antioxidánsokat pulzálva is lehet szedni, pl. a délutáni időszakra korlátozva a C és E vitamint, mert az oxidációs folyamatoknak is fontos szerepe van az anyagcsere és immunműködés szempontjából. Az E-vitamin és karotinoidok nagy dózisban nem javasoltak, inkább polifenolok (Étrendi források és táplálékkiegészítők).
- A Q10 vitamin: Antioxidáció, mind a membrán terápia, cukor bontásából származó acetilcsoport mitokondriumba szállításában van szerepe. A szervezet elő tudja állítani fenilalaninból és tirozinból, de az előállított mennyiség az életkorral csökken. A fehérje emésztés nehezítettsége, ill. nitrostressz esetén a tirozin mennyisége csökken, ill. tönkre megy (nitrotirozin), így a Q10 termelés is összeomolhat.
- Antioxidáns vitaminok, kofaktorok: D, A, K vitaminok, C-vitamin, magnézium, szelén, cink, réz, B vitaminok stb.
- Növényi hatóanyagok, szín-, ízanyagok: Polifenolok, kurkumin, rezveratrol, quercetin...
- Mangán (A mitokondriális beépített antioxidációt a szuperoxid dizmutáz SOD enzim végzi, mangánnal működik) (Laborkontroll fontos, mert a túl sok mangán toxikus: teljes vér/hajszövetanalízis!!)
A mitokondriális membránokat (is) támogató hatóanyagok:
- Foszfatidilkolin/kolin, étrendi forrás: Tojássárgája, kolin
- Foszfatidilszerin/szerin, glicinből átalakul, étrendi szerin források: Velő, belsőségek, Étrendi glicin források: Kollagén jellegű állati szövetek
- EPA/DHA min 2 g/nap. Magas oxidatív terhelés esetén oxidálódhat (Esetenként második lépésben, antioxidánsokkal való feltöltést követően!!) Étrendi megoldásként: zsíros tengeri halak, halolajak működhetnek.

A mitokondriális működés különböző folyamatait támogatják még a biotin, B1 vitamin (optimálisan benfotiamin formában), a B2, B3 vitaminok, a B12 vitamin adenozil formája, a kreatin, taurin, az alfa liponsav, és rengeteg növényi hatóanyag, melyek olívabogyóban, feketeáfonyában, gránátalmában, brokkoliban stb. vannak. Fontos az is, hogy a mitokondriális működés károsodását okozó folyamatok azonosítva legyenek. Ilyenek a gócbetegségek, vagy egyéb krónikus infekciók, toxikus hatások (pl. amalgám fogtömések, amit csak megfelelően képzett szakemberrel javaslunk eltávolíttatni, aki gondoskodik a megfelelő védelemről az eltávolítás során), tápanyag- és vitamin hiányok, életmódtényezők.
A tünetei mögötti okokat keresi?
A funkcionális megközelítés segít megérteni, mi áll a panaszok hátterében — és személyre szabott tervet ad ahhoz, hogy újra jól érezze magát.
Konzultáció foglalásaTetszett a cikk? Iratkozz fel hírlevelünkre →
Források
2 forrásokForrások
[1] U. Gröber, Arzneimittel und Mikronährstoffe: medikationsorientierte Supplementierung. Wiss. Verlag-Ges., 2018. [2] B. Kuklinski, Mitochondrien : Symtome, Diagnose und Therapie. Aurum Verlag, 2015.